Die antimikrobielle Wirksamkeit von Wasserstoffperoxid ist seit etwa 100 Jahren bekannt, im Bereich der Kontaktlinsenhygiene wird sie seit etwa 20 Jahren genutzt. Ihre abtötende Wirkung beruht auf der oxidativen Zerstörung wichtiger Zellkomponenten durch hochaktiven Sauerstoff, so genannte „Sauerstoffradikale“, die bei der Zersetzung von Wasserstoffperoxid entstehen. Innerhalb von 20 Minuten werden alle augenpathogenen Mikroorganismen wirksam inaktiviert, wenn über den ganzen Zeitraum eine 3%ige Konzentration aufrechterhalten bleibt.
Bei der Arbeit kennt Peroxid keine Kompromisse!
Ein wichtiger Indikator der antimikrobiellen Wirksamkeit ist die Inaktivierung von Acanthamoeba. Acanthamoeben sind ubiquitär freilebende Protozoen (Einzeller). Die wichtigsten augenpathogenen Vertreter sind Acanthamoeba culbertsoni, Acanthamoeba polyphaga und Acanthamoeba castellani. Man findet sie im Wasser (sowohl Salzwasser, Quellwasser, Leitungswasser und Trinkwasser), in der Luft, im Erdreich und auch im menschlichen Speichel[2].
Als Protozoen sind Acanthamöben Einzeller, die man den Eukaryonten zurechnet. Sie gelten als Erreger diverser Krankheiten, wie beispielsweise auch der Amöbenruhr, die durch Entamoeba histolytica über verseuchtes Trinkwasser übertragen wird. In der Ophthalmologie sind sie verantwortlich für die „Acanthamöben-Keratitis“, einer schweren Infektion des Auges.
Seit Beginn der 80er Jahre des vergangenen Jahrhunderts richtet sich das ophthalmologische Augenmerk besonders in den USA und in Großbritannien auf Acanthamoeben: in erster Linie werden sie durch kontaminierte weiche Kontaktlinsen übertragen werden können und hier schwerste Hornhauterkrankungen hervorrufen können. Acanthamoeben verfügen über ein sehr gutes Anhaftungsvermögen an Kunststoffe. Bereits nach 10 sekündigen Abspülen mit einer mit Acanthamoeba-kontaminierten Lösung sind auf Kontaktlinsen Acanthamoeben nachweisbar[3].
 Acanthamoeba – Trophozoit[4]
Acanthamoeba – Trophozoit[4]
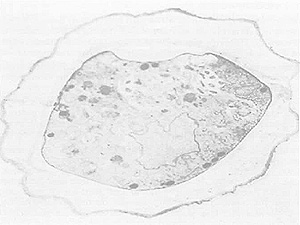 Acanthamoeba Zyste[4]
Acanthamoeba Zyste[4]
Charakteristisch für diese einzelligen Lebewesen ist der freilebende und vermehrungsfähige Trophozoit als vegetative Form und das abgekapselte Ruhe- oder Zysten-Stadium als Überdauerungsform. Der Trophozoit kann sich problemlos aktiv fortbewegen und vermehren, er ernährt sich hauptsächlich von Bakterien. Unter ungünstigen Umweltbedingungen wandelt sich der Trophozoit in eine Zyste um. Diese Zyste besitzt als sehr resistente Überdauerungsform eine äußerst dicke Zellwand, die die ruhende Acanthamöbe vor widrigen Einflüssen schützt.
Der bevorzugte Lebensraum von Acanthamoeben ist das Wasser: Sie treten bevorzugt in stehenden Gewässern, in Leitungswasser, chloriertem Badewasser und destilliertem Wasser auf. Ebenfalls sind sie in Tafelwasser, Quellwasser und Salzwasser zu finden. Die übliche Aufbereitung des Trinkwassers reicht nicht zur Dekontamination aus, da Acanthamoeben einer Desinfektion mit Chlor widerstehen können. Leitungswasser ist besonders dann durch Acathamoeben bedroht, wenn es entweder kalt ist, es aus Vorratsbehältern oder Wassercontainern stammt oder wenn es Kalkbestandteile aufweist. In London wurden in 2% aller Trinkwasserproben und 14% aller Badewasserproben Acanthamoeben nachgewiesen[5]. Darüber hinaus sind Acanthamoeben auch am Ausfluss von Wasserhähnen nachweisbar – deshalb ist Leitungswasser zum Abspülen von Kontaktlinsen absolut tabu.
Die durch Acanthamoeben hervorgerufene Acanthamoeben-Keratitis stellt eine Infektion dar, die am Auge schlimmstenfalls bis zur Erblindung führen kann. Eine erste Augeninfektion mit Acanthamöben wurde bereits 1974 beschrieben[6] – wobei es sich hier nicht um einen Kontaktlinsenträger handelte. Ende der 80er Jahre des vergangenen Jahrhunderts wurden in den USA bereits 208 und in Europa 60 Fälle beschrieben[7], ist Zahl steigt weiter an[8].
|
Risiko Acanthamoeba Die wissenschaftlich anerkannten Risikofaktoren für die Übertragung von Acanthamöben stellen im Wesentlichen folgende Ursachen dar: |
- Abspülen der Kontaktlinsen mit Leitungswasser
- Aufbewahren und Benutzen kontaminierter Kochsalzlösungen
- Mangelhaft durchgeführte Reinigung und Desinfektion der Kontaktlinsen
- Befeuchten der Kontaktlinsen mit Speichel
- Schwimmen in allen Gewässern
- Duschen während des Tragens der Kontaktlinsen
Der Infektionsmechanismus der Hornhaut wird in der Literatur kontrovers diskutiert: Acanthamöben scheinen entweder über Mikroabrasionen oder auch selbständig die Cornea zu infiltrieren.
Kontaktlinsendesinfektion
Die antimikrobielle Wirksamkeit von Wasserstoffperoxid als sichere Art der Desinfektion ist in zahlreichen Publikationen dokumentiert. So schrieb Moore[9], dass eine wirksame Desinfektion gegen Acanthamoeba-Trophozoiten und –Zysten zum einen durch Hitzedesinfektion bei 70 – 80°C für 10 Minuten, zum anderen durch 3%iges Wasserstoffperoxid gesichert wird. Dies wurde von Davies[10] im selben Jahr bestätigt. Da Hitzedesinfektion einen hohen Materialstress für Kontaktlinsen darstellt und etwaige Ablagerungen bei dieser Prozedur festbacken können, stellt Wasserstoffperoxid zum Abtöten aller pathogenen Keime eine sichere und materialschonende Alternative dar. Ebenfalls im Jahr 1990 bestätigte Anger[11], dass 3%iges Wasserstoffperoxid ein ausgezeichnetes antimikrobielles Agens sei, doch nur wenn die Konzentration nicht zu schnell auf weniger als 1% absinkt. Sonst ist nur eine unzureichende Desinfektion der Kontaktlinsen wahrscheinlich, denn die Acanthamoeben-Zysten werden nur nach einer längeren Einwirkzeit von 3%igem Wasserstoffperoxid abgetötet. Die Neutralisation des Wasserstoffperoxids muss also zeitverzögert stattfinden.
Auch Wilson und Botzenhart berichteten über die Effektivität von Wasserstoffperoxidsystemen in der Kontaktlinsenhygiene, da sie auch Biofilme erfolgreich angreifen[12,13]. Wasserstoffperoxid bietet somit die Grundlage für ein ausgezeichnetes antimikrobielles Kontaktlinsenhygienesystem.
Wirksamkeit von Kontaktlinsenpflegemitteln gegenüber Acanthamoeben
Im Annex D der Norm ISO/DIS 14729 „Augenoptik – Kontaktlinsenpflegemittel – Mikrobiologische Anforderungen und Prüfverfahren für Produkte und Systeme zum Hygienemanagement von Kontaktlinsen“ wird auf Sinn- und Zweckmäßigkeit einer Prüfung von Kontaktlinsenpflegemitteln auch auf Acanthamoeba speziell eingegangen.
Hier wird erwähnt, dass…
- Acanthamoeba-Infektionen sehr selten auftreten
- zur Abtötung der Zysten in der Regel nur stark antimikrobiell wirksame Substanzen fähig sind, die wiederum toxisch am Auge sein können
- das Wachstum von Acanthamoeben durch die Präsenz von Bakterien gefördert wird
- es keine standardisierten Testmethoden zur Prüfung auf Acanthamoeben gibt, welche die Art, das Entwicklungsstadium, die Anzahl der überlebenden Organismen und die Wiederfindungsraten berücksichtigt
Bei der Beurteilung der Aussagekraft von mikrobiologischen Studien hierzu ist beispielsweise besonders der letzte Punkt zu beachten. Um aussagekräftige Ergebnisse zu präsentieren, müssen Testmethoden nachvollziehbare valide Techniken und Ansätze verwenden. Für alle verwendeten Test-Produkte müssen somit gleiche Bedingungen vorliegen um eindeutig vergleichbare Aussagen zu ermöglichen. Dazu gehört auch beispielsweise die Benutzung derselben Laborgeräte für die zu vergleichenden Parameter. Praxisrelevant ist darüber hinaus die Verwendung einer realistischen Menge an Keimen, die in etwa dem tatsächlichen Vorkommen entsprechen soll. Studienergebnisse, die diesen grundlegenden Anforderungen nicht entsprechen, liefern keine verläßlichen Ergebnisse und sorgen mehr für Konfusiuon als für wissenschaftliche Klärung.
Acanthamoeben stellen einen äußerst widerstandsfähigen Keim dar. Allein die antimikrobielle Wirksamkeit des Desinfektionssystemes zu erhöhen kann nicht Sinn einer sicheren und wirksamen Kontaktlinsenhygiene sein – die Abtötung von Acanthamoeba-Zysten wird ohnehin selten erreicht und mit der Erhöhung bzw. Wahl des keimtötenden Agens kann eine schädliche Wirkung für Kontaktlinse und Auge verbunden sein.
Ganz besonders im Zusammenhang mit der Vorbeugung vor Acanthamoeben-Infektionen am Auge ist eine grundsätzliche Betrachtung allgemeiner Hygieneempfehlung äußerst sinnvoll:
- Verwenden Sie niemals Leitungswasser
- Verwenden Sie Desinfektionslösungen immer nur ein Mal
- Beachten Sie die Hygienevorschriften der Hersteller.
Wasserstoffperoxid
Bei Verwendung von Wasserstoffperoxidsystemen in der Kontaktlinsenhygiene ist eine „Neutralisation“ des Peroxides unverzichtbar. Wasserstoffperoxid kann auf sehr einfacher Art und Weise inaktiviert werden. Bei diesem rückstandsfreien Neutralisationsprozess entstehen Wasser und Sauerstoff. Somit bieten Wasserstoffperoxidsysteme die Möglichkeit die Kontaktlinsen direkt nach einer höchst effizienten Desinfektion aus einer unkonservierten Lösung aufzusetzen. Diese Form der Kontaktlinsenhygiene leistet somit einen weiteren wesentlichen Beitrag zur Gesundheit am Auge[14].
| 2 H2O2 => 2 H2O + O2
Neutralisation von Wasserstoffperoxid |
Anwenderfreundlichkeit und Sicherheit – unvereinbar?
Klassische 2-Schritt-Peroxidsysteme kamen der Forderung nach Anwenderfreundlichkeit nur unzureichend nach. Der Wunsch nach „Einfachheit“ und gleichzeitiger „Sicherheit“ wurde mit der Einführung von Ein-Schritt-Peroxidsystemen beantwortet.
Technisch ist dies auf zweierlei Weg möglich:
- Platinkatalytische Neutralisation des Peroxides
Hier wird ein Platinkatalysator zur Neutralisation des Peroxides verwendet. Wichtig zu wissen ist hierbei, dass bei metallkatalytischen Systemen die Neutralisation sofort beginnt, sobald die Lösung in den Behälter eingefüllt wird und sie beim Schließen Kontakt mit dem Platinkatalysator erhält. Die 3%ige Peroxidkonzentration nimmt dabei sofort ab, was eine reduzierte Desinfektionswirksamkeit zur Folge haben kann[15]. Durch Abnutzungserscheinungen kann die Leistungsfähigkeit des Katalysators nachlassen, was zu Restkonzentrationen in der Lösung und somit zu Irritationen am Auge führen kann[4]. - Biokatalytische Neutralisation mit ummantelten Tabletten
Anders wirken Ein-Schritt-Peroxidsysteme, die das Peroxid durch die zeitverzögerte Freisetzung des Biokatalysators aus einer Tablette neutralisieren. Die biokatalytische Neutralisation erfolgt mit dem Enzym Katalase, das in geringsten Konzentrationen schnell und effektiv das Wasserstoffperoxid restlos neutralisiert[16] und so Irritationen effizient ausschließt.
Durch die Nutzung moderner Galenik verhindert ein Cellulosemantel, der das Enzym umhüllt, den vorzeitigen Eintritt der Wirkung. Diese Substanz wird ebenfalls in Benetzungs- und Nachbenetzungslösungen verwendet und trägt somit auch zur Steigerung der Spontanverträglichkeit bei. Vitamin B12 als Anwendungskontrolle der Zugabe der Neutralisationstablette in manchen Tabletten ermöglicht darüber hinaus eine optische Kontrolle auch wirklich nichts vergessen zu haben.
Gerade bei der Inaktivierung von Acanthameoben ist Wasserstoffperoxid unübertroffen[17]. In ihrer Studie aus dem Jahr 2001 beschreiben Kilvington und Anger[18] die Beeinflussung der Desinfektionsleistung von Kontaktlinsenpflegemitteln gegenüber Acanthamöben in Abhängigkeit vom Reifegrad der Zysten. Das hier getestete 1-stufige Wasserstoffperoxid-System, das mit einer 3%-gen Peroxid-Konzentration über ca. 20 min desinfiziert, erreicht bei der anschließenden Neutralisationszeit von 6h sogar eine effektive Abtötung aller Acanthamoeben-Entwicklungsstadien.
Infektionen am Auge durch Acanthamöben stellen eine zwar seltene, allerdings sehr ernst zu nehmende Erkrankung dar, die unbedingt vermieden werden muss. In Bezug auf die Kontaktlinsenhygiene können diese Infektionen – wie auch Infektionen mit anderen pathogenen Keimen – durch die Einhaltung der wesentlichen Hygienemaßnahmen vermieden werden. Auch die Einhaltung der Herstellerempfehlung für Kontaktlinsenpflegemittel stellt hierfür die Basis dar.
 Amöbenkongress, Larson, G., Katzenwäsche, München 1990
Amöbenkongress, Larson, G., Katzenwäsche, München 1990
Autorin:
Dr. Magda Rau, Privatklinik Dr. Magda Rau
Janahof 2
D-93413 Cham/Janahof
info@augenklinik-cham.de
Literatur und Bildquellen:
[1] Coverfoto am Kopf des Artikels: www.augeninfo.de/bild_db/index.php?alle=1&suchen=1 (Abgriff 30.05.2007)
[2] Berke A., Scholtz S., Trinkwasser: Anmerkungen zur Kontaktlinsenpflege, DOZ, 3 und 4 / 1999.
[3] Berke A., Scholtz S., Trinkwasser: Anmerkungen zur Kontaktlinsenpflege, DOZ, 3 und 4 / 1999.
[4] Berke, A., Blümle, S., Kontaktlinsenhygiene, Bode-Verlag, 1. Auflage.
[5] Hay J; Seal DV; Kirkness CM ., Acanthamoeba keratitis: A water-borne disease, J. Med. Mikrobiol. 41 (suppl.), 290, 1994.
[6] Nagington J., Watson P., Payfair T., McGill J., Jones B., Steele A., „Amoebic infection of the eye“, Lancet, 2:1537 – 1540, 1974.
[7] Colin J., Malet F., Robinet A., Heitz R., The Epidemiology of Acanthamoeba Keratitis in Europe, Contactologia 12-54-56, 1990.
[8] Stehr-Green J., Bailey T., Visvesvara G., The epidemiology of acanthamoeba keratitis in the United States, Amer. J. Ophthalmol. 107:331 – 336, 1989
[9] Moore, 1990
[10] Davies et al., A new concept in contact lens disinfection, The Optician, 199 (5429), 1990.
[11] Anger et al., Antimicobial Efficacy of Hydrogen Peroxide for Contact Lens Disinfection, Contact Lens Spectrum, 11, 46-51, 1990.
[12] Wilson L.A., et al., Comparative efficacies of soft Contact Lens Disinfectant solutions against microbial films in lens cases, Arch. Ophthalmol, 109 (8), 1991.
[13] Scholtz, S., Ott, H., Biofilm, Focus, 5/2004, S. 48 – 51.
[14] Scholtz, S., Ott, Hans H., Wasserstoffperoxid in der Kontaktlinsenhygiene – Desinfektion und mehr! Die Kontaktlinse, 09/2003, S. 23 – 26.
[15] Davies, et al., Evaluation of the Anti-Acanthamoebal Activity of five Contact Lens Disinfectants, ICLC, Vol 17., Jan/Feb.1990.
[16] Gyulai et al., Relative neutralisation ability of six hydrogen peroxide disinfection systems, Contact Lens Spectrum, 1987, 2, 61-8.
[17] Kilvington S., Anger C., A comparison of cyst age and assay method of the efficacy of contact lens disinfectants against Acanthamoeba, Br J Ophthalmol, 2001; 85, 336 – 340.
[18] Kilvington S., Anger C., A comparison of cyst age and assay method of the efficacy of contact lens disinfectants against Acanthamoeba, Br J Ophthalmol, 2001; 85, 336 – 340.
[19] Larson, G., Katzenwäsche, München 1990.




